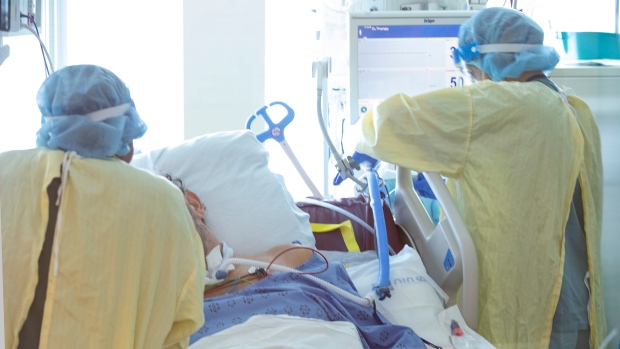
Vaccins COVID-19 pour enfants : La FDA va examiner les demandes de Pfizer et Moderna
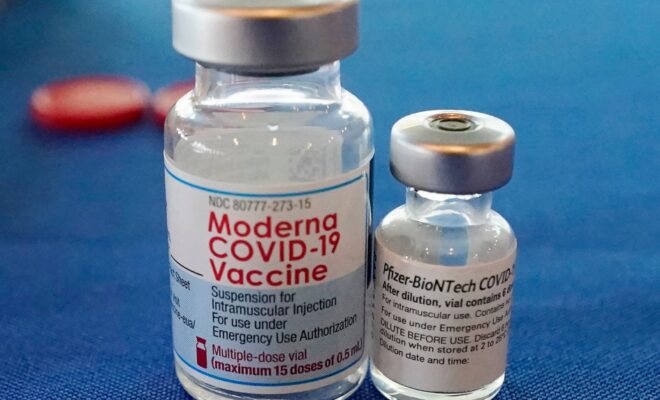
La Food and Drug Administration américaine a fixé les 14 et 15 juin comme nouvelle date de réunion pour examiner la demande d’autorisation d’urgence de Moderna Inc pour son vaccin COVID-19 destiné aux enfants âgés de 6 mois à 5 ans et le vaccin de Pfizer Inc pour ceux âgés de 6 mois à 4 ans.
Les nouvelles dates des réunions de notre comité consultatif sur le vaccin pédiatrique COVID-19 seront désormais les 14 et 15 juin, a déclaré la FDA dans un communiqué lundi.
« Nous savons que les parents ont hâte que nous déterminions si ces vaccins sont sûrs & ; efficaces. A la lumière des informations fournies par Pfizer concernant leurs données et les dates prévues de soumission, nous pensons pouvoir achever l’examen des deux demandes d’autorisation européenne de mise sur le marché à quelques jours d’intervalle », a déclaré la FDA.
La réunion du 14 juin examinera la demande d’autorisation d’utilisation en urgence de Moderna pour les jeunes âgés de six à 17 ans, a déclaré la FDA.
Le Dr Ashish Jha, coordinateur de la réponse au COVID-19 à la Maison Blanche, a déclaré dimanche qu’il s’attendait à une décision de la Food and Drug Administration américaine concernant l’autorisation du vaccin Moderna pour les enfants de moins de cinq ans dans les prochaines semaines.
Moderna a complété sa demande et les experts de la FDA examinent de près les données, a déclaré Jha sur ABC.
(Reportage de Doina Chiacu ; édition de Mark Porter et Nick Zieminski)