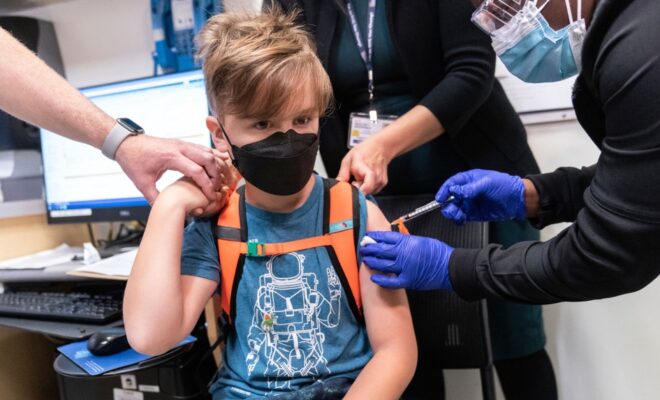
Les enfants doivent attendre plus longtemps entre les doses du vaccin COVID-19 de Pfizer au Canada qu’aux États-Unis.
TORONTO — Le Canada maintiendra un intervalle de trois semaines entre les doses du vaccin COVID-19 de Pfizer-BioNTech pour les enfants âgés de cinq à 11 ans, malgré une recommandation de porter cet intervalle à huit semaines.
Vendredi, Santé Canada a autorisé le vaccin Pfizer pour les enfants, ce qui en fait le premier du pays à recevoir une approbation réglementaire pour ce groupe d’âge. Un total de 2,9 millions de doses devraient arriver d’ici la fin de la semaine prochaine.
Bien que Santé Canada et Pfizer affirment que le vaccin peut être administré à trois semaines d’intervalle, le Comité consultatif national de l’immunisation (CCNI) a recommandé un intervalle de huit semaines entre les doses.
Le CCNI note que, bien qu’il n’y ait pas de preuve directe d’un intervalle optimal pour les enfants, il cite des preuves chez les adultes qu’un intervalle plus long peut améliorer la réponse immunitaire.
« Nous constatons que le CCNI a formulé une recommandation différente sur la base de sa propre analyse des données « , a déclaré Fabien Paquette, responsable des vaccins chez Pfizer Canada, à CTV News.
« Donc, au bout du compte, que ce soit du point de vue du CCNI ou de celui des provinces, c’est à elles qu’il revient d’appliquer les programmes de vaccination de la manière qui leur semble la plus appropriée pour leur population. »
M. Paquette a indiqué qu’à la suite de discussions avec les autorités fédérales, notamment la Food and Drug Administration (FDA) des États-Unis, un intervalle de trois semaines a été convenu pour les programmes cliniques de Pfizer, comme c’était le cas pour les adolescents et les adultes.
A la question de savoir si cela ferait une différence dans l’efficacité du vaccin, il a répondu que les données ne sont pas disponibles.
« Ce que nous avons dans nos propres ensembles de données est vraiment un intervalle de trois semaines. Un intervalle plus long n’a pas été étudié pour ce groupe d’âge », a-t-il déclaré.
« Maintenant, nous pouvons faire des hypothèses sur la base de ce que nous avons vu dans les groupes d’adultes, et c’est probablement la façon dont l’analyse a été faite par les autorités de santé publique. Mais par rapport à ce que nous voyons actuellement, les données disponibles sont vraiment avec un intervalle de trois semaines. »
M. Paquette a déclaré qu’il est trop tôt pour dire si les vaccins pédiatriques pour le COVID-19 seront offerts annuellement, mais que davantage de données seront recueillies pour s’assurer que « les meilleures décisions seront prises à cet égard. »
M. Paquette a également qualifié l’autorisation de Santé Canada de » jour que de nombreux parents à travers le pays attendaient avec impatience » et de » changement de donne » probable pour protéger davantage les Canadiens contre le COVID-19.
Il a déclaré que Pfizer a soumis une quantité » importante » de données à Santé Canada, notamment pour les essais de phase 2 et 3, auxquels ont participé plus de 4 600 enfants, avec une efficacité de 91 % et peu d’effets secondaires.
Il a déclaré qu’aucun cas de myocardite, un effet secondaire observé avec les vaccins à ARNm entraînant une inflammation du muscle cardiaque, n’a été signalé au cours des essais cliniques. Mais il a ajouté que Pfizer prend la question au sérieux et sera attentif à tous les rapports qui seront publiés au fur et à mesure que les vaccins seront utilisés au Canada et dans le monde.
Interrogé sur les parents qui hésitent à faire vacciner leur enfant, M. Paquette a répondu que c’était « tout à fait compréhensible ».
« Si vous avez des enfants âgés de cinq à douze ans, vous voulez ce qu’il y a de mieux pour eux, et ce qu’il y a de mieux pour eux, d’après ce que nous voyons actuellement avec les données scientifiques disponibles, c’est clairement de leur présenter un vaccin qui a été officiellement autorisé par Santé Canada. Et je vous dirais de parler à vos fournisseurs de soins de santé « , a-t-il ajouté.
En ce qui concerne les mandats de vaccination pour les enfants, M. Paquette a déclaré que ce n’est pas à une société pharmaceutique de répondre, mais plutôt aux autorités de santé publique.