Vaccin COVID pour les enfants de moins de 6 ans au Canada : Moderna demande l’approbation
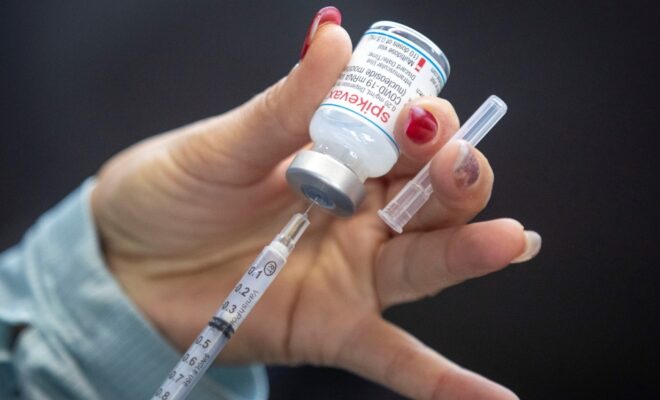
Moderna dit qu’elle travaille sur une soumission à Santé Canada pour l’approbation d’un vaccin COVID-19 pour les enfants de moins de six ans.
La société de biotechnologie a demandé jeudi aux régulateurs américains d’autoriser de faibles doses de son vaccin pour les enfants âgés de six mois à cinq ans.
Cette décision tant attendue est une autre étape vers des tirs potentiellement ouvrants pour des millions de tout-petits d’ici l’été.
Au Canada, Moderna dit espérer terminer la demande d’approbation réglementaire de son vaccin COVID-19, Spikevax, « sous peu ».
À ce jour, Santé Canada n’a approuvé que les vaccins à ARNm contre la COVID-19 pour les enfants de plus de cinq ans.
Le vaccin Pfizer-BioNTech, Comirnaty, est disponible pour les enfants de 5 à 11 ans, et Moderna Spikevax est disponible pour les enfants de 6 à 11 ans. Selon les données fédérales, environ 41 % des enfants canadiens de cette cohorte ont reçu deux vaccins.
Des familles frustrées attendent avec impatience une chance de protéger les plus petits enfants alors que tout autour d’eux, les gens jettent des masques et d’autres précautions de santé publique – même si des mutants de coronavirus hautement contagieux continuent de se propager.
Déjà environ les trois quarts des enfants américains de tous âges montrent des signes qu’ils ont été infectés à un moment donné pendant la pandémie.
Au Canada, les données fédérales indiquent que 10,8 % des cas signalés concernaient des enfants de moins de 11 ans.
Moderna a soumis des données à la Food and Drug Administration qui, espère-t-elle, prouveront que deux injections à faible dose peuvent protéger les bébés, les tout-petits et les enfants d’âge préscolaire – mais pas aussi efficacement pendant la poussée d’Omicron qu’au début de la pandémie.
« Il y a un important besoin médical non satisfait ici avec ces plus jeunes enfants », a déclaré le Dr Paul Burton, médecin-chef de Moderna, à l’Associated Press. Deux injections pour enfants « les protégeront en toute sécurité. Je pense qu’il est probable qu’avec le temps, ils auront besoin de doses supplémentaires. Mais nous y travaillons. »
Désormais, seuls les enfants âgés de cinq ans ou plus peuvent être vaccinés aux États-Unis, en utilisant le vaccin du rival Pfizer, laissant 18 millions de jeunes enfants sans protection.
Le vaccin de Moderna n’est pas le seul dans la course. Pfizer devrait bientôt annoncer si trois de ses doses encore plus petites fonctionnent pour les plus petits, des mois après la découverte décevante que deux doses n’étaient pas assez fortes.
Qu’il s’agisse des vaccins d’une entreprise ou des deux, le chef des vaccins de la FDA, le Dr Peter Marks, a déclaré que l’agence « agira rapidement sans sacrifier nos normes » pour décider si les doses tot sont sûres et efficaces.
Alors que les questions tourbillonnent sur ce qui prend si longtemps, Marks a clairement déclaré aux législateurs plus tôt cette semaine que la FDA ne peut pas évaluer un produit tant qu’un fabricant n’a pas terminé sa demande. Dans un communiqué jeudi, la FDA a déclaré qu’elle organiserait une réunion pour débattre publiquement des preuves de Moderna avec ses conseillers scientifiques indépendants, mais que la société doit encore soumettre des données supplémentaires. Moderna prévoit de le faire d’ici quelques semaines.
« Il est extrêmement important que nous ayons la bonne évaluation afin que les parents aient confiance dans tous les vaccins que nous autorisons », a déclaré Marks à un comité sénatorial.
Si la FDA autorise les vaccinations pour les plus petits, les Centers for Disease Control and Prevention devraient ensuite recommander qui en a besoin – tous les tout-petits ou seulement ceux qui sont plus à risque de COVID-19.
« Il est très important de faire vacciner les plus jeunes enfants », mais « agir rapidement ne signifie pas agir négligemment », a déclaré le Dr Philip Landrigan, pédiatre et expert en santé publique au Boston College. La FDA doit « voir si c’est sûr. Ils doivent voir si c’est efficace. Et ils doivent le faire rapidement. Mais ils ne feront pas de compromis. »
De nombreux parents recherchent désespérément le vaccin qui atteindra en premier la ligne d’arrivée scientifique.
« Nous avons été en quelque sorte laissés pour compte alors que tout le monde passe à autre chose », a déclaré Meagan Dunphy-Daly, une biologiste marine de l’Université Duke dont la fille de six ans est vaccinée – mais dont la fille de trois ans et de 18 mois- fils âgés font partie du procès de Pfizer.
La famille continue de masquer et de prendre d’autres précautions jusqu’à ce qu’il soit clair si les garçons ont reçu un vrai vaccin ou des injections factices. S’il s’avère qu’ils n’étaient pas protégés dans l’étude de Pfizer et que les vaccins de Moderna sont effacés en premier, Dunphy-Daly a déclaré qu’elle les chercherait pour ses fils.
« Je ressentirai un tel soulagement quand je saurai que mes garçons sont vaccinés et que le risque qu’ils contractent une infection grave est si faible », a-t-elle déclaré.
La FDA sera confrontée à des questions complexes.
Dans une étude portant sur des enfants âgés de six mois à cinq ans, deux injections de Moderna – chacune représentant le quart de la dose habituelle – ont déclenché des niveaux élevés d’anticorps anti-virus, la même quantité prouvée pour protéger les jeunes adultes, a déclaré Burton. Il n’y a pas eu d’effets secondaires graves et les injections ont déclenché moins de fortes fièvres que les autres vaccinations de routine.
Mais le vaccin s’est avéré efficace entre environ 40 et 50 % pour prévenir le COVID-19 symptomatique pendant l’essai. Burton a blâmé la capacité de la variante Omicron à échapper partiellement à l’immunité vaccinale, notant que les adultes non boostés montraient de la même manière moins d’efficacité contre les infections plus légères à Omicron. Bien qu’aucun enfant ne soit tombé gravement malade au cours de l’étude, il a déclaré que des niveaux élevés d’anticorps sont un indicateur de protection contre des maladies plus graves – et la société testera une dose de rappel pour les enfants.
« Ce n’est pas totalement hors du domaine de ce à quoi nous nous attendions », a déclaré le Dr Bill Muller de l’Université Northwestern, qui a aidé aux études sur les enfants de Moderna. « Plus tard, je prévois que ce sera une série en trois coups. »
Autre problème : jusqu’à présent aux États-Unis, le vaccin de Moderna est réservé aux adultes. D’autres pays ont étendu le tir aux enfants dès l’âge de six ans. Mais alors que Moderna a également déposé des demandes auprès de la FDA pour les enfants plus âgés, la FDA n’a pas statué sur eux. Il y a des mois, l’agence a fait part de son inquiétude concernant un effet secondaire rare, l’inflammation cardiaque, chez les adolescents, une préoccupation qui n’a pas été signalée chez des enfants beaucoup plus jeunes.
Il n’est pas clair si la FDA envisagera le vaccin de Moderna pour les enfants de tous âges maintenant ou se concentrera d’abord sur les plus petits. Mais Muller a déjà demandé à de nombreux parents pourquoi les vaccins étaient testés chez les tout-petits avant les enfants plus âgés – et dit que les pédiatres et les pharmaciens doivent être prêts avec des réponses.
Burton a déclaré que les données de sécurité de millions d’enfants plus âgés ayant reçu des vaccins Moderna à l’étranger devraient aider à rassurer les parents.
Bien que le COVID-19 ne soit généralement pas aussi dangereux chez les jeunes que chez les adultes, certains tombent gravement malades ou même meurent. Environ 475 enfants de moins de cinq ans sont morts du COVID-19 depuis le début de la pandémie, selon le CDC, et les hospitalisations d’enfants ont grimpé en flèche au pic d’Omicron.
Pourtant, on ne sait pas combien de parents ont l’intention de vacciner les plus jeunes enfants. Moins d’un tiers des enfants âgés de 5 à 11 ans ont reçu deux vaccins, et 58 % de ceux âgés de 12 à 17 ans.
— Avec des fichiers de l’Associated Press
Ce rapport de La Presse canadienne a été publié pour la première fois le 28 avril 2022.