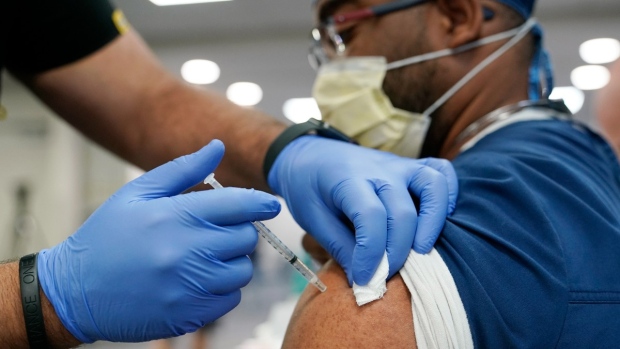
Lécanemab : médicament contre la maladie d’Alzheimer approuvé aux États-Unis ; ce que cela signifie pour le Canada
Le premier médicament à ralentir la progression de la maladie d’Alzheimer a été approuvé aux États-Unis, et le Canada pourrait suivre bientôt.
Le lecanemab, également connu sous le nom de marque Leqembi, est le premier traitement disponible pour la maladie d’Alzheimer en Amérique du Nord.
Donald Weaver, directeur et chercheur principal à l’Institut de recherche Krembil du Réseau universitaire de santé, a déclaré vendredi à CTV Your Morning que ce médicament modificateur de la maladie n’est pas un remède mais « un pas dans la bonne direction ».
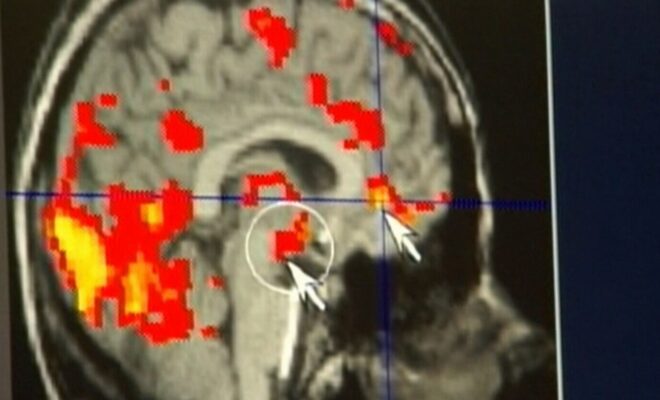
Weaver a expliqué que Leqembi se lie et empêche la protéine amyloïde de s’agglutiner et de s’accumuler dans le cerveau.
« Il y a beaucoup de gens qui pensent que l’amyloïde est la clé de ce qui cause la maladie d’Alzheimer », a-t-il déclaré.
Weaver a ajouté lors de l’étude du médicament, il a montré une amélioration de la mémoire de 27% qu’il a comparée à l’expansion des capacités et des fonctions cognitives de six mois.
« Vous pourrez peut-être rester à la maison six mois de plus. Vous pourrez peut-être reconnaître et interagir avec votre famille à un niveau plus significatif », a-t-il déclaré, « C’est une quantité de temps énorme. »
En 2020, 597 300 personnes vivraient avec la maladie d’Alzheimer ou un autre type de démence au Canada, et plus de 950 000 devraient recevoir un diagnostic de la maladie d’ici 2030, selon la Société Alzheimer Canada.
Le médicament nouvellement approuvé ne fonctionne que sur certaines personnes.
Weaver a déclaré qu’il devait être pris soit aux « très premiers stades » de la maladie d’Alzheimer, soit avant une déficience cognitive légère, ce qui signifie que les personnes atteintes de formes plus avancées de la maladie d’Alzheimer pourraient ne pas en bénéficier.
Une étude de 18 mois publiée en novembre 2022 a révélé que le médicament pouvait entraîner un risque d’effets secondaires graves pour certains patients, près de 13 % des 1 795 personnes ayant participé à l’essai ayant subi des effets secondaires tels qu’un gonflement du cerveau ou des saignements.
Bien que la récente approbation de la FDA américaine n’ait pas d’impact sur les Canadiens pour le moment, Weaver a déclaré que leur expérience aidera d’autres pays à prendre une décision. Lecanemab a été soumis pour approbation par Santé Canada en mai.