Santé Canada en » phase finale » de l’examen du médicament antiviral COVID-19 de Pfizer

Le Dr Supriya Sharma, médecin-conseil en chef de Santé Canada, déclare que l’agence en est aux dernières étapes de l’examen du traitement antiviral prometteur de Pfizer.
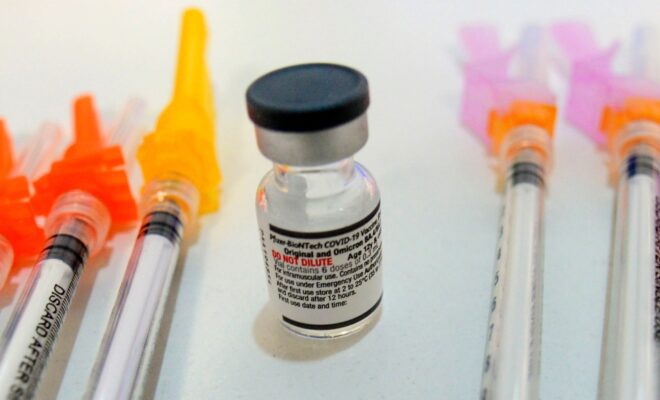
Pfizer a soumis les données cliniques de son médicament Paxlovid le 1er décembre 2021.
« Nous sommes dans les dernières étapes de l’examen. Je ne peux pas m’engager sur une date précise, mais nous aurons probablement une décision à ce sujet d’ici une semaine à dix jours « , a déclaré M. Sharma dans une déclaration à CTVNews.ca.
Le fabricant de médicaments a déclaré dans un communiqué de presse que la pilule est conçue pour bloquer l’activité d’une enzyme dans le SRAS-CoV-2 qui est essentielle pour que le virus se réplique, et aussi pour aider à ralentir la dégradation des ingrédients de la pilule afin d’aider à combattre le virus plus longtemps. Une partie de la pilule utilise le ritonavir, un médicament existant qui a déjà été utilisé en combinaison avec d’autres médicaments antiviraux.
Les provinces et les territoires ont demandé au gouvernement fédéral d’accélérer le processus d’approbation, plus récemment avec l’augmentation de la variante Omicron hautement transmissible.
Cependant, l’agence a clairement indiqué les étapes à franchir pour qu’un médicament soit approuvé au Canada – étapes qui ne changent pas sous la pression politique.
« Santé Canada n’autorisera l’utilisation de traitements antiviraux que si l’examen scientifique indépendant et approfondi de toutes les données incluses dans les soumissions montre que les avantages des traitements l’emportent sur les risques potentiels », a déclaré Mark Johnson, porte-parole de Santé Canada.
Le ministre fédéral de la Santé, Jean-Yves Duclos, a déclaré aux journalistes mercredi, lors d’une mise à jour sur le COVID-19, que l’examen se poursuivait « rapidement, de manière accélérée ».
« Ils travaillent évidemment avec des partenaires internationaux pour s’assurer que cela avance rapidement et efficacement. L’annonce et la décision seront faites très bientôt. Alors que nous nous préparons à cette décision, quelle qu’elle soit, nous avons déjà obtenu un million de doses de vaccin contre le VIH. [Pfizer’s] traitement », a-t-il déclaré.
M. Duclos a ajouté qu’il a eu plusieurs conversations avec ses homologues provinciaux et territoriaux pour s’assurer que, si le traitement est approuvé, le gouvernement fédéral est prêt à passer rapidement à l’utilisation clinique.
Santé Canada examine également une pilule expérimentale du fabricant de médicaments Merck, appelée molnupiravir, soumise le 13 août.
Le gouvernement a signé un accord pour un maximum de 500 000 unités du médicament molnupiravir, avec une option pour 500 000 unités supplémentaires.
Fin décembre, la Food and Drug Administration américaine a émis une autorisation d’utilisation d’urgence pour les médicaments de Pfizer et de Merck.
Avec un dossier d’Alexandra Mae Jones de CTV News.