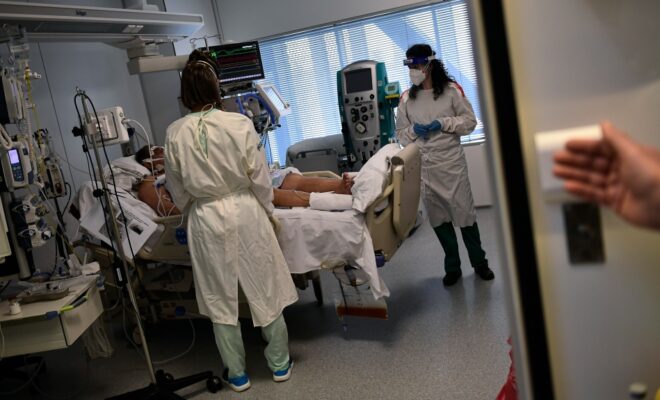
Pfizer teste une injection supplémentaire de COVID-19 pour les enfants de moins de 5 ans, ce qui constitue un échec

LAURAN NEERGAARD — Pfizer a annoncé vendredi qu’il changeait ses plans et testait trois doses de son vaccin COVID-19 chez les bébés et les enfants d’âge préscolaire, les deux doses habituelles n’ayant pas semblé assez fortes pour certains enfants.
Pfizer a annoncé ce changement après qu’une analyse préliminaire ait révélé que les enfants de 2 à 4 ans n’ont pas eu une réponse immunitaire aussi forte que prévu aux doses très faibles que la société teste chez les plus jeunes enfants.
Ce sont des nouvelles décevantes pour les familles impatientes de faire vacciner leurs enfants. Pfizer espérait obtenir des données sur l’efficacité des vaccins chez les enfants de moins de 5 ans d’ici la fin de l’année, et on ne sait pas combien de temps ce changement retardera la réponse finale.
Pfizer et son partenaire BioNTech ont déclaré que si l’étude à trois doses est concluante, ils prévoient de demander une autorisation d’urgence au cours du premier semestre 2022.
Une version pour enfants du vaccin de Pfizer est déjà disponible pour les enfants de 5 à 11 ans, une version qui représente un tiers de la dose administrée à toute personne de 12 ans et plus.
Pour les enfants de moins de 5 ans, Pfizer teste une dose encore plus petite, de seulement 3 microgrammes, soit un dixième de la dose pour adultes.
Les chercheurs ont analysé un sous-ensemble d’enfants participant à l’étude, un mois après leur deuxième dose, pour voir si les enfants avaient développé des niveaux d’anticorps anti-virus similaires à ceux des adolescents et des jeunes adultes qui reçoivent les vaccins habituels.
Les injections à très faible dose ont semblé fonctionner chez les enfants de moins de 2 ans, qui ont produit des niveaux d’anticorps similaires. Mais la réponse immunitaire chez les enfants de 2 à 4 ans était inférieure à ce que l’étude exigeait, a déclaré vendredi Kathrin Jansen, responsable de la recherche sur les vaccins chez Pfizer, lors d’une conférence téléphonique avec les investisseurs.
Plutôt que d’essayer une injection à dose plus élevée pour les enfants d’âge préscolaire, Pfizer a décidé d’étendre l’étude pour évaluer trois des injections à très faible dose chez tous les participants à l’étude – de 6 mois à 5 ans. Cette troisième injection aura lieu au moins deux mois après la deuxième dose des enfants.
Aucun problème de sécurité n’a été détecté dans l’étude, ont déclaré les entreprises.
Jansen a cité d’autres données montrant qu’une injection de rappel pour les personnes de 16 ans et plus restaure une forte protection, un saut dans l’immunité qui, les scientifiques l’espèrent, aidera également à repousser la nouvelle variante omicron.
Les entreprises se préparent également à tester un rappel pour les enfants de 5 à 11 ans, qui commencent tout juste à recevoir leurs deux doses de vaccin. Et elles testent différentes options de doses pour les rappels destinés aux adolescents.
Mme Jansen a déclaré que si les tests pédiatriques supplémentaires étaient concluants, « nous aurions une approche cohérente du vaccin à trois doses pour tous les âges ».