La FDA approuve le vaccin COVID-19 pour enfants aux Etats-Unis ; le Canada devrait suivre de près.
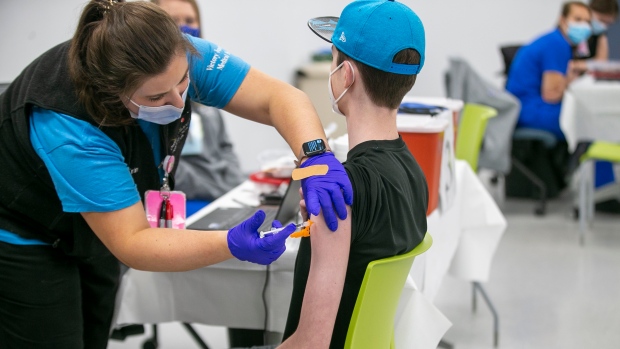
OTTAWA — Le Canada surveille de près la Food and Drug Administration des États-Unis maintenant qu’elle a approuvé le vaccin COVID-19 de Pfizer-BioNTech pour les enfants âgés de cinq à onze ans.
La FDA a approuvé le vaccin pour une utilisation d’urgence vendredi après-midi, citant des données qui montrent que le vaccin est efficace à 90 % pour prévenir le COVID-19 chez les enfants et qu’il n’y a pas eu d’effets secondaires graves.
Le comité consultatif de la FDA a recommandé d’approuver le vaccin après des heures de témoignages d’experts mardi.
Des représentants de Santé Canada ont assisté à cette réunion et suivent attentivement le processus aux États-Unis, alors que le Canada prend sa propre décision concernant le vaccin pédiatrique.
« Ces délibérations et ces discussions seront également prises en compte dans notre examen « , a déclaré le Dr Supriya Sharma, conseillère médicale en chef de Santé Canada, lors d’une séance d’information vendredi.
Santé Canada a reçu la demande d’approbation de Pfizer-BioNTech et les données connexes un peu plus tard que la FDA, et les fonctionnaires canadiens sont toujours en train de l’examiner.
« Nos scientifiques sont en train d’examiner non seulement les résultats des essais cliniques et des études qui ont été réalisés, mais aussi les détails de la nouvelle formulation « , a déclaré M. Sharma.
Le vaccin pédiatrique COVID-19 diffère légèrement de la formulation adulte de Pfizer-BioNTech. Pour cette raison, la société devra livrer de nouveaux flacons du vaccin avant que les enfants canadiens puissent recevoir leur injection.
Le Canada attend 2,9 millions de doses de taille enfant de la nouvelle formulation si elle est approuvée, soit suffisamment pour que chaque enfant reçoive sa première dose.
Mais M. Sharma a déclaré qu’il pourrait encore s’écouler quelques semaines avant que Santé Canada ne prenne une décision finale.
« Nous avons reçu la semaine dernière des informations supplémentaires que nous sommes en train d’examiner « , a déclaré M. Sharma.
« Je pense que les choses se passent très bien. Je ne vois pas de décision avant la mi ou la fin novembre. »
La FDA et les centres américains de contrôle et de prévention des maladies surveilleront le déploiement des vaccins pour enfants afin de déceler tout effet indésirable, et les responsables canadiens de la santé publique garderont également un œil sur ces données.
Le CDC se réunira la semaine prochaine pour discuter des recommandations cliniques concernant l’administration du vaccin pour enfants aux États-Unis.
Pendant ce temps, Santé Canada attend d’autres soumissions pour les vaccins pédiatriques dans les semaines à venir.
Moderna soumettra « bientôt » une demande pour un vaccin pédiatrique, selon Patricia Gauthier, directrice générale de Moderna Canada.
Les données provisoires de Moderna pour son vaccin destiné aux enfants de six à onze ans montrent un solide profil de sécurité ainsi qu’une forte réponse immunitaire, a déclaré Mme Gauthier lors d’un événement public organisé par The Canadian Club mardi.
« Nous avons maintenant besoin d’une analyse future, mais ces données sont très positives et nous permettent maintenant d’avoir des conversations avec Santé Canada et de commencer à penser à cette soumission « , a-t-elle déclaré.
Ce rapport de la Presse canadienne a été publié pour la première fois le 29 octobre 2021.