Des questions subsistent sur le médicament contre la maladie d’Alzheimer
Le lecanemab, un médicament expérimental contre la maladie d’Alzheimer, a fait la une des journaux la semaine dernière lorsque les sociétés qui l’ont testé ont publié des résultats d’essais qui ont montré que le médicament avait atteint ses objectifs, ce qui en fait l’un des premiers médicaments contre la démence à donner des résultats positifs.
Dans une étude randomisée et contrôlée par placebo portant sur près de 1 800 personnes qui en étaient aux premiers stades de la perte de mémoire, celles qui prenaient du lecanemab présentaient environ 27 % de déclin en moins après 18 mois que celles qui n’en prenaient pas, ont indiqué les sociétés. La différence s’élevait à environ un demi-point sur une échelle couramment utilisée appelée Évaluation clinique de la démence – Somme des cases. La différence était statistiquement significative, indiquant que l’amélioration n’était probablement pas due au hasard.
Les entreprises n’ont donné qu’un aperçu de l’étude dans un communiqué de presse, et les experts disent qu’ils voudront approfondir les détails avant d’avoir une compréhension complète des résultats.
Mais s’il réussit, lecanemab aura résisté à une longue histoire d’échecs sur le terrain.
QU’EST-CE QUI EST DIFFÉRENT CETTE FOIS ?
Selon certains comptes, le lecanemab est le 16e médicament développé pour éliminer les plaques amyloïdes toxiques du cerveau. Beaucoup d’autres ont également travaillé comme annoncé; ils ont enlevé l’amyloïde. Le hic, c’est que presque aucun n’a montré de réel avantage pour les patients, ce qui a conduit de nombreux experts à conclure que tout le champ était, eh bien, dans le champ gauche.
Ils ont déclaré fausse la soi-disant hypothèse amyloïde – l’idée que les plaques amyloïdes s’accumulent dans le cerveau et sont une cause de la maladie d’Alzheimer – et ont appelé les développeurs de médicaments à retourner à la planche à dessin.
Donc, après cette longue série d’échecs, pourquoi le lecanemab a-t-il l’air d’avoir fonctionné ? Y a-t-il quelque chose dans le médicament qui le rend meilleur? Ou les entreprises qui le testent – Biogen et Eisai – ont-elles mené un essai clinique plus intelligent qui a finalement montré le potentiel de ces types de médicaments ?
« C’est en fait une combinaison des deux », a déclaré le Dr Michael Irizarry, directeur clinique adjoint d’Eisai pour la maladie d’Alzheimer et la santé du cerveau.
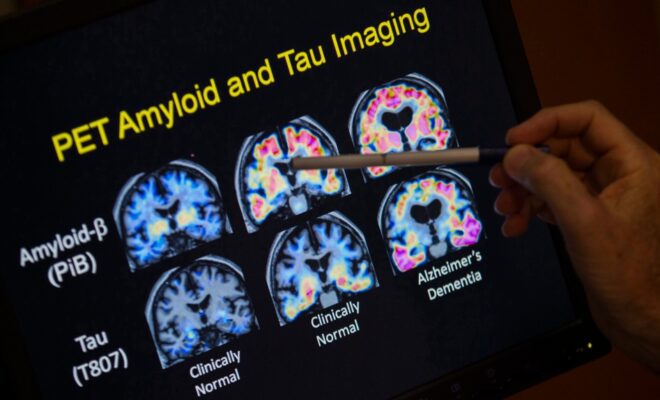
Irizarry a déclaré qu’en planifiant l’essai clinique, les chercheurs ont pu tirer parti des avancées technologiques, comme de nouveaux types d’analyses qui peuvent confirmer la présence de bêta-amyloïde dans le cerveau. Auparavant, les médecins ne pouvaient voir l’amyloïde dans le cerveau que lors des autopsies.
Ils ont recruté des personnes qui étaient plus tôt au cours de leur maladie, à un moment où des agents comme le lecanemab pourraient potentiellement faire du bien.
« Nous nous sommes assurés de recruter des personnes dans les essais cliniques qui ont la cible et pourraient être en mesure de répondre au médicament », a déclaré Irizarry.
Ils ont également pu apprendre des faux pas avec les traitements précédents, comme l’aducanumab, qui est également fabriqué par Biogen et Eisai. Ils ont inclus près de 1 800 personnes dans la dernière étape de l’essai clinique, suffisamment pour montrer une différence entre le groupe prenant le médicament et le groupe ayant reçu un placebo.
Irizarry dit que les chercheurs ont également utilisé leur essai de phase 2 pour choisir avec soin le dosage, et donc dans la phase 3, tous les participants assignés au hasard à la thérapie ont reçu la même dose.
Enfin, dit Irizarry, tous les anticorps qui ciblent l’amyloïde s’y accrochent à des endroits légèrement différents. Le lecanemab se lie à ces morceaux de protéines lorsqu’ils se sont réunis pour former des chaînes de morceaux d’amyloïde appelés protofibrilles, mais avant que ces chaînes ne s’agglutinent pour former des plaques dans le cerveau. Il se pourrait que la capture de l’amyloïde plus tôt dans le processus fasse également une différence.
EN ATTENTE DE PLUS DE DONNÉES
Cependant, certains experts indépendants doutent qu’il s’agisse d’une grande percée.
« Je ne pense pas que nous constatons un avantage clinique si différent de l’aducanumab », a déclaré le Dr Constantine Lyketsos, psychiatre et professeur à la Johns Hopkins School of Medicine.
Aducanumab, vendu sous le nom d’Aduhelm, a été approuvé par la Food and Drug Administration des États-Unis en juin 2021, malgré les objections du panel de conseillers externes de l’agence. Les résultats des essais cliniques étaient mitigés, un seul montrant un petit avantage pour les patients. Medicare a accepté de couvrir le médicament uniquement dans certaines circonstances, et c’est devenu un flop commercial.
« La principale différence est que le lecanemab avait une taille d’échantillon beaucoup plus grande », a déclaré Lyketsos.
Si vous superposez les résultats observés avec le lecanemab à ceux observés avec l’aducanumab dans l’étude où il a montré un résultat positif, dit-il, vous verriez à peu près le même degré de bénéfice.
« Je pense que nous assistons à une approche stratégique réussie par les entreprises qui la développent pour avoir une très grande étude suffisamment importante pour détecter un petit effet », a-t-il déclaré.
Lyketsos s’inquiète également du gonflement du cerveau appelé ARIA, abréviation d’anomalies d’imagerie liées à l’amyloïde. Ces effets secondaires ont été observés avec d’autres types d’anticorps éliminant l’amyloïde et sont survenus chez environ 1 participant sur 5 prenant du lécanemab.
Les protofibrilles ciblées par le médicament tapissent les parois des vaisseaux sanguins du cerveau, a-t-il déclaré. Lorsqu’ils sont retirés, les vaisseaux peuvent laisser échapper du liquide ou du sang dans le cerveau. Si suffisamment de fuites, cela apparaît sur une IRM.
Certaines personnes qui reçoivent ARIA ne présentent aucun symptôme. Mais parfois, ils peuvent être plus graves, entraînant une hospitalisation ou une déficience durable.
Lyketsos dit que les experts ne comprennent pas encore ce qui se passe lorsque des ARIA légers vont et viennent à plusieurs reprises ou à quel point un cas catastrophique de gonflement du cerveau peut être courant.
Si le lecanemab n’a été perfusé que chez quelques milliers de personnes, il se peut que l’échantillon ne soit pas suffisamment important pour savoir si des cas de gonflement cérébral plus grave peuvent apparaître comme des événements rares.
« Peut-être qu’il n’y a pas une telle catastrophe. Nous ne savons tout simplement pas », a-t-il déclaré. « Donc, beaucoup de médicaments comme celui-ci, s’ils devaient arriver sur le marché, auraient ce gros astérisque à côté qui indique que nous ne savons vraiment rien de la sécurité à long terme. »
Lyketsos dit qu’il serait vraiment difficile d’offrir le lecanemab à un patient.
« Si c’était une simple pilule, si ce n’était pas très cher, je pourrais », a-t-il déclaré. Mais étant donné le coût probable du médicament – l’aducanumab, par exemple, coûte maintenant environ 28 000 dollars pour un an de traitement – et le léger ralentissement de la progression de la maladie, ce serait difficile.
Le prix du lecanemab ne sera annoncé que s’il est approuvé par la FDA.
Il dit qu’il pourrait changer d’avis si l’analyse de l’essai clinique montre qu’un groupe de personnes a obtenu plus d’avantages que d’autres.
Irizarry d’Eisai dit que la société analyse actuellement les résultats des essais pour ce problème précis – si les personnes présentant des risques génétiques pour la maladie d’Alzheimer, ou peut-être celles souffrant de problèmes de santé compliqués comme le diabète ou l’hypertension artérielle, peuvent avoir réagi différemment au traitement.
« C’est définitivement un domaine sur lequel nous travaillons », a-t-il déclaré.
AVANTAGE OU BIAIS ?
D’autres experts craignent que l’essai ait été faussé parce que ces événements ARIA – qui ne se produisent que chez les personnes qui reçoivent des anticorps anti-amyloïdes – ont essentiellement révélé aux médecins et aux patients qu’ils recevaient le médicament, annulant ainsi l’insu de l’étude.
La principale mesure utilisée pour évaluer les participants à l’étude était une enquête qui classe dans quelle mesure ils fonctionnent dans six domaines de leur vie, y compris la mémoire, l’orientation et la résolution de problèmes. Elle repose, en grande partie, sur l’évaluation de l’aidant principal de la personne.
« C’est très sujet aux biais », a déclaré le Dr Michael Greicius, neurologue et professeur à l’Université de Stanford.
« De toute évidence, tout le monde veut que les patients aillent mieux – les patients, les soignants, les cliniciens – et c’est pourquoi nous nous appuyons très fortement sur cette notion de double aveugle afin que personne ne sache si vous recevez un traitement actif ou un placebo », a-t-il déclaré. a dit.
Les personnes recevant le traitement – qui est administré par perfusion IV une fois toutes les deux semaines – peuvent avoir des réactions telles que des tremblements, des frissons et une fièvre légère.
Greicius dit que personne n’a trouvé de solution pour masquer les participants à l’étude à ces effets secondaires très importants, qui nécessitent que les participants obtiennent des scanners cérébraux supplémentaires et interrompent leurs traitements.
« Je veux être convaincu que cela déplace réellement l’aiguille, mais j’ai besoin de voir un peu plus de preuves pour cela », a-t-il déclaré.
Un autre expert pense que le lecanemab peut fonctionner dans une certaine mesure, mais pas pour les raisons que les gens supposent.
Le Dr Alberto Espay, neurologue à l’Université de Cincinnati, affirme qu’en plus d’éliminer la bêta-amyloïde du cerveau, le lecanemab augmente les niveaux de la version normale de la protéine amyloïde, appelée AB42.
Cette version de la protéine fait partie intégrante de la structure et de la fonction du cerveau, dit-il, et ses études ont montré que sa perte est plus étroitement corrélée au déclin cognitif, plutôt qu’à l’accumulation de plaques amyloïdes. Cependant, il admet que cette idée n’est pas une théorie dominante dans la recherche sur la maladie d’Alzheimer.
Espay dit qu’il n’envisagerait jamais de donner ce type de médicaments à ses patients, non seulement parce que leurs avantages sont faibles, mais aussi parce que les coûts pourraient être effarants. Si des millions de personnes y sont mises, nous en paierons tous le prix, dit-il.
En novembre, Medicare a annoncé qu’elle augmentait les primes mensuelles de son plan Partie B, en partie à cause de ses dépenses prévues pour l’aducanumab.
Dans une déclaration envoyée par e-mail à CNN, Eisai dit qu’il n’a pas encore fixé le prix du lecanemab, mais qu’il est sensible aux préoccupations concernant le coût du médicament.
« Aux États-Unis, l’approche d’Eisai en matière de tarification sera basée sur un cadre de modélisation qui prend en compte les résultats de l’essai Clarity AD, en tenant compte de la durabilité du système de santé et d’un niveau d’abordabilité pour les personnes vivant avec une AD précoce », porte-parole a écrit Christopher Vancheri.
Ces médicaments « vont casser le système de santé », a déclaré Espay. « S’ils étaient vraiment bons pour les patients, alors oui, cassons le système de santé, car cela va faire une différence.
« Cela ne peut pas faire de différence. »